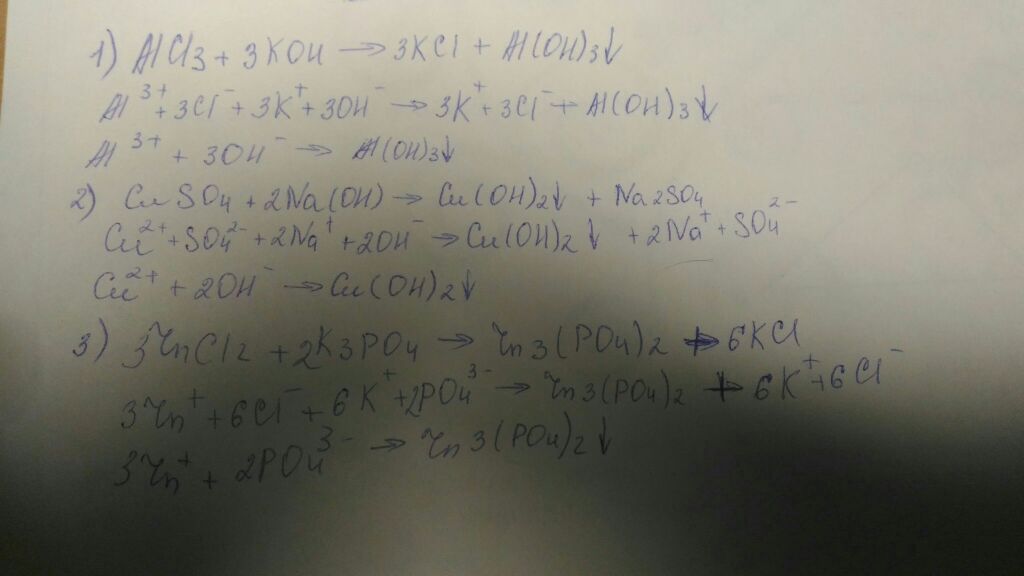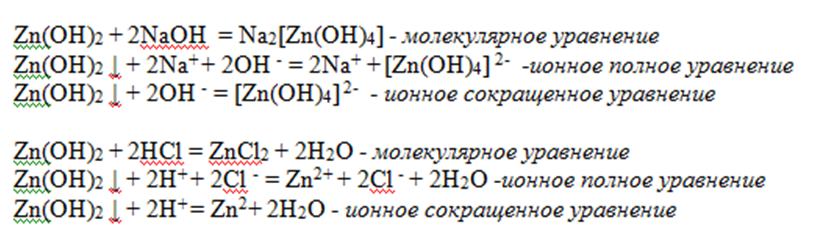 Решенное и коэффициентами уравнение реакции cuso4 + 2 koh → k2so4 + cu(oh)2 с дополненными продуктами. Приложение для вычисления и дополнения продуктов реакции.
Решенное и коэффициентами уравнение реакции cuso4 + 2 koh → k2so4 + cu(oh)2 с дополненными продуктами. Приложение для вычисления и дополнения продуктов реакции.
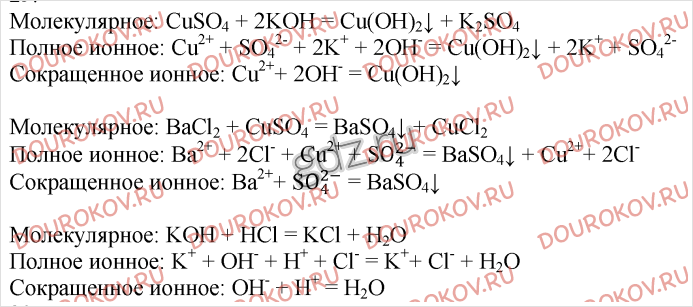
 Реакция протекает между такими веществами как основание гидроксид калия и соли сульфата меди. В результате реакции обмена образуются два вещества так же …
Реакция протекает между такими веществами как основание гидроксид калия и соли сульфата меди. В результате реакции обмена образуются два вещества так же …
 При нагревании хлората калия (KClO3) в присутствии катализатора часть вещества …
При нагревании хлората калия (KClO3) в присутствии катализатора часть вещества …
 1 cuso 4 + 1 koh = 1 cu(oh) 2 + 1 k 2 so 4 For each element, we check if the number of atoms is balanced on both sides of the equation. Cu is balanced: 1 atom in reagents and 1 atom in …
1 cuso 4 + 1 koh = 1 cu(oh) 2 + 1 k 2 so 4 For each element, we check if the number of atoms is balanced on both sides of the equation. Cu is balanced: 1 atom in reagents and 1 atom in …
 1 cuso 4 + 1 koh = 1 cu(oh) 2 + 1 k 2 so 4 Для каждого элемента мы проверяем, сбалансировано ли количество атомов в обеих частях уравнения. cu сбалансирован: 1 …
1 cuso 4 + 1 koh = 1 cu(oh) 2 + 1 k 2 so 4 Для каждого элемента мы проверяем, сбалансировано ли количество атомов в обеих частях уравнения. cu сбалансирован: 1 …
 Узнайте, какой тип реакции необходим. Уравняйте CuSO4 + KOH = Cu (OH)KSO4 химическое уравнение или реакцию с помощью этого калькулятора!
Узнайте, какой тип реакции необходим. Уравняйте CuSO4 + KOH = Cu (OH)KSO4 химическое уравнение или реакцию с помощью этого калькулятора!
 CuSO4 + KOH = K2SO4 + Cu(OH)2 is a Double Displacement (Metathesis) reaction where one mole of aqueous Cupric Sulfate [CuSO 4] and two moles of aqueous Potassium Hydroxide …
CuSO4 + KOH = K2SO4 + Cu(OH)2 is a Double Displacement (Metathesis) reaction where one mole of aqueous Cupric Sulfate [CuSO 4] and two moles of aqueous Potassium Hydroxide …
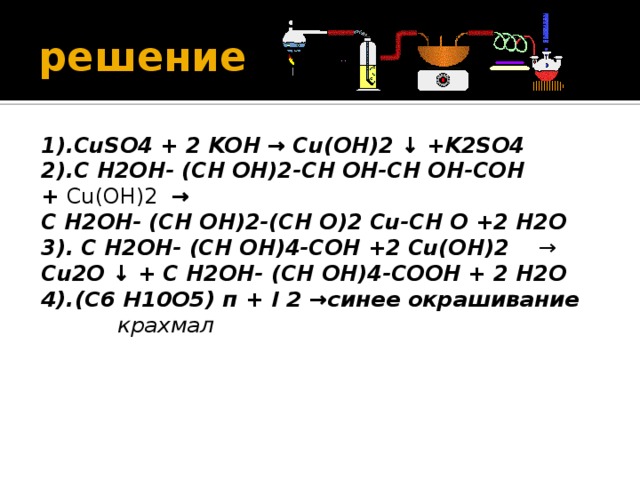 Уравнение реакции взаимодействия сульфата меди (II) с гидроксидом калия. Получение сульфата калия и гидроксида меди (II) из сульфата меди (II) и гидроксида калия.
Уравнение реакции взаимодействия сульфата меди (II) с гидроксидом калия. Получение сульфата калия и гидроксида меди (II) из сульфата меди (II) и гидроксида калия.
 Купрум со4 - это соль, обладающая кислотными свойствами. Его химическая формула CuSO4 указывает на то, что оно состоит из ионов меди (Cu2+) и ионов …
Купрум со4 - это соль, обладающая кислотными свойствами. Его химическая формула CuSO4 указывает на то, что оно состоит из ионов меди (Cu2+) и ионов …
 Сульфа́т меди (II) (медь (II) серноки́слая, традиционное название кристаллогидрата — ме́дный купоро́с) — неорганическое соединение, медная соль серной кислоты с …
Сульфа́т меди (II) (медь (II) серноки́слая, традиционное название кристаллогидрата — ме́дный купоро́с) — неорганическое соединение, медная соль серной кислоты с …
 Ag + CuSO 4 → реакция не идет, так как серебро стоит правее меди в ряду активностей металлов и, следовательно, является более слабым металлом. 2. Соли вступают в …
Ag + CuSO 4 → реакция не идет, так как серебро стоит правее меди в ряду активностей металлов и, следовательно, является более слабым металлом. 2. Соли вступают в …
 Избыток сильной кислоты приводит к разрушению комплекса и образованию двух средних солей и воды: Na[Al(OH) 4] + 4HCl (изб.) = NaCl + AlCl 3 + 4H 2 O,
Избыток сильной кислоты приводит к разрушению комплекса и образованию двух средних солей и воды: Na[Al(OH) 4] + 4HCl (изб.) = NaCl + AlCl 3 + 4H 2 O,
 В ЕГЭ было замечено только взаимодействие гидросульфата с магнием в растворе, поэтому нужно быть очень аккуратным с этими реакциями: NaHSO₄ + Mg → MgSO₄ + …
В ЕГЭ было замечено только взаимодействие гидросульфата с магнием в растворе, поэтому нужно быть очень аккуратным с этими реакциями: NaHSO₄ + Mg → MgSO₄ + …
Еще по теме:












Еще по теме: