Ответ: массовая доля выхода анилина составляет 61,7%. При восстановлении 12,3г нитробензола было получено 8,5 г анилина. Рассчитайте массовую долю выхода - ответ …
Ответ: массовая доля выхода анилина составляет 61,7%. При восстановлении 12,3г нитробензола было получено 8,5 г анилина. Рассчитайте массовую долю выхода - ответ …
 При восстановлении 12,3 г нитробензола получили 6,5 г анилина. Рассчитайте массовую долю выхода продукта реакции от теоретически возможного.
При восстановлении 12,3 г нитробензола получили 6,5 г анилина. Рассчитайте массовую долю выхода продукта реакции от теоретически возможного.
 При восстановлении 12,3 г нитробензола получили 6,5 г анилина. Рассчитайте массовую долю выхода продукта реакции от теоретически возможного.
При восстановлении 12,3 г нитробензола получили 6,5 г анилина. Рассчитайте массовую долю выхода продукта реакции от теоретически возможного.
 При восстановлении 12,3 г нитробензола получили 6,5 г анилина. Рассчитайте массовую долю выхода продукта реакции от теоретически возможного.
При восстановлении 12,3 г нитробензола получили 6,5 г анилина. Рассчитайте массовую долю выхода продукта реакции от теоретически возможного.
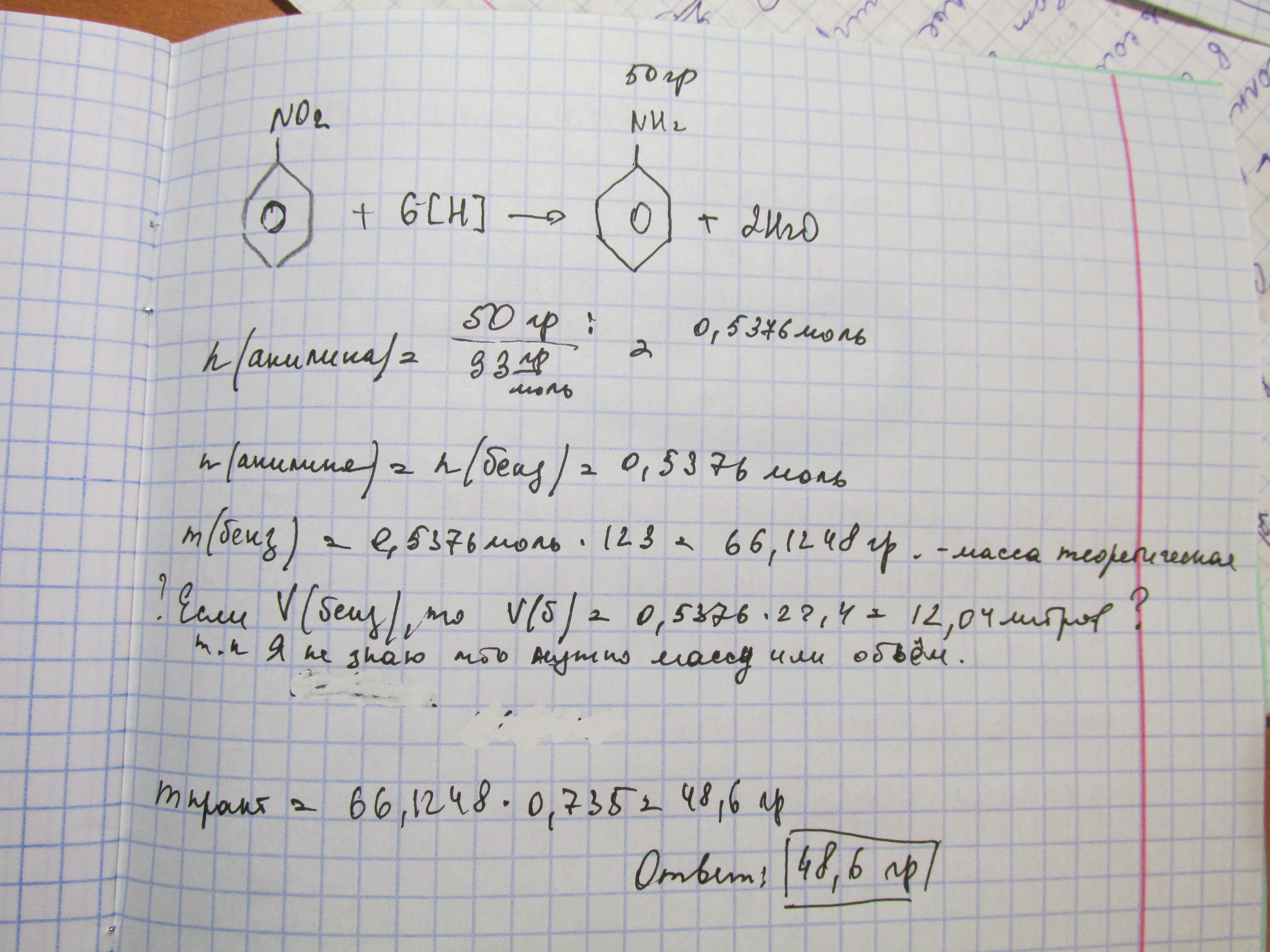 Рассчитайте массу анилина который можно получить при восстановлении нитробеозола массой 246г, если массовая доля выхода продукта 90%.
Рассчитайте массу анилина который можно получить при восстановлении нитробеозола массой 246г, если массовая доля выхода продукта 90%.
 Смесь бензола и циклогексана дегидрировали над платиновым катализатором, при этом выделилось такое количество водорода, которое может …
Смесь бензола и циклогексана дегидрировали над платиновым катализатором, при этом выделилось такое количество водорода, которое может …
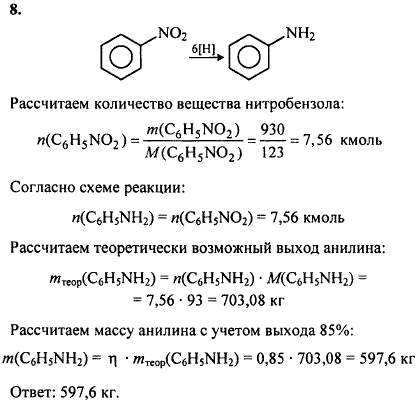
 Уравнение реакции восстановления нитробензола до анилина: c 6 h 5 no 2 + 6[h] = c 6 h 5 nh 2 + 2h 2 o. Количество вещества нитробензола: v(c 6 h 5 no 2) = m(c 6 h 5 no 2)/m(c 6 h …
Уравнение реакции восстановления нитробензола до анилина: c 6 h 5 no 2 + 6[h] = c 6 h 5 nh 2 + 2h 2 o. Количество вещества нитробензола: v(c 6 h 5 no 2) = m(c 6 h 5 no 2)/m(c 6 h …
 При восстановлении 12,3 г нитробензола было получено 8,5 г анилина. Рассчитайте массовую долю выхода анилина. Смотреть ответ
При восстановлении 12,3 г нитробензола было получено 8,5 г анилина. Рассчитайте массовую долю выхода анилина. Смотреть ответ
 Рассчитаем количество вещества нитробензола: n = m/M = 12,3г/123г/моль = 0,1моль. По уравнению реакции: n(C6H5NH2) = n(C6H5NO2) = 0,1моль. Рассчитаем масса 0,1моль …
Рассчитаем количество вещества нитробензола: n = m/M = 12,3г/123г/моль = 0,1моль. По уравнению реакции: n(C6H5NH2) = n(C6H5NO2) = 0,1моль. Рассчитаем масса 0,1моль …
 При восстановлении 37 грамм нитробензола в присутствии водорода образовалось 18, 5 грамм анилина. Рассчитайте выход анилина (в%) по сравнению с теоретически …
При восстановлении 37 грамм нитробензола в присутствии водорода образовалось 18, 5 грамм анилина. Рассчитайте выход анилина (в%) по сравнению с теоретически …
 1. Восстановление нитробензола протекает по уравнению: c 6 h 5 no 2 + 3h 2 → c 6 h 5 nh 2 + 2h 2 o; 2. Рассчитаем химическое количество нитробензола: n (c 6 h 5 no 2) = m (c 6 h 5 …
1. Восстановление нитробензола протекает по уравнению: c 6 h 5 no 2 + 3h 2 → c 6 h 5 nh 2 + 2h 2 o; 2. Рассчитаем химическое количество нитробензола: n (c 6 h 5 no 2) = m (c 6 h 5 …
 Рассмотрим вариант решения задания из учебника Рудзитис, Фельдман 10 класс, Просвещение: 6. При восстановлении 250 г нитробензола получили 150 г анилина. …
Рассмотрим вариант решения задания из учебника Рудзитис, Фельдман 10 класс, Просвещение: 6. При восстановлении 250 г нитробензола получили 150 г анилина. …
 При восстановлении 12,3 г нитробензола было получено 8,5 г анилина. Рассчитайте массовую долю выхода анилина. Посмотрите правильный ответ!
При восстановлении 12,3 г нитробензола было получено 8,5 г анилина. Рассчитайте массовую долю выхода анилина. Посмотрите правильный ответ!
 3. Находим массу теоретическую для продукта, выход от теоретически возможного: m (C 6 H 5 NH 2 ) = Y * M = 0,1 * 93 = 9,3 г;
3. Находим массу теоретическую для продукта, выход от теоретически возможного: m (C 6 H 5 NH 2 ) = Y * M = 0,1 * 93 = 9,3 г;
 При восстановлении 250 г нитробензола получили 150 г анилина. Вычислите, сколько это составляет процентов по сравнению с теоретическим выходом продукта реакции.
При восстановлении 250 г нитробензола получили 150 г анилина. Вычислите, сколько это составляет процентов по сравнению с теоретическим выходом продукта реакции.
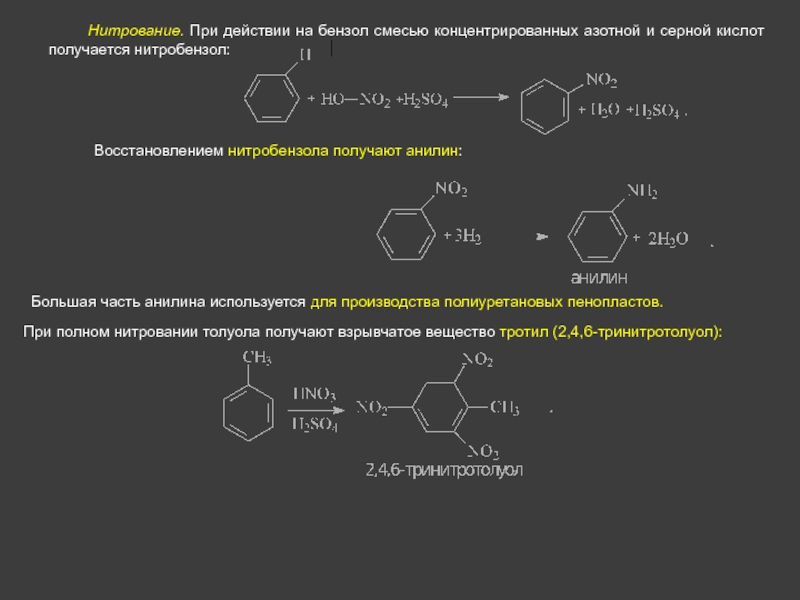
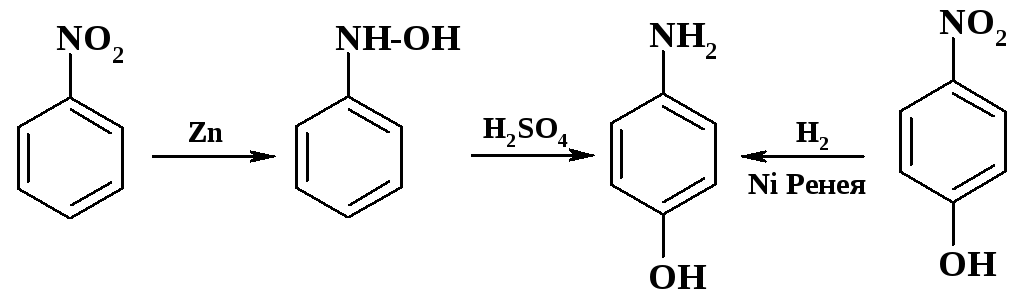
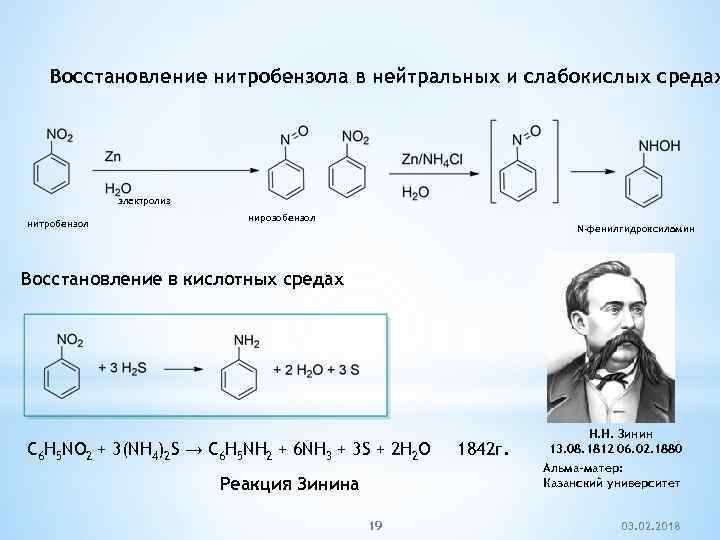
 В лабораторных условиях восстановление нитробензола можно проводить железными стружками, цинком или оловом в присутствии соляной кислоты, либо алюминием или …
В лабораторных условиях восстановление нитробензола можно проводить железными стружками, цинком или оловом в присутствии соляной кислоты, либо алюминием или …
Еще по теме:













Еще по теме: