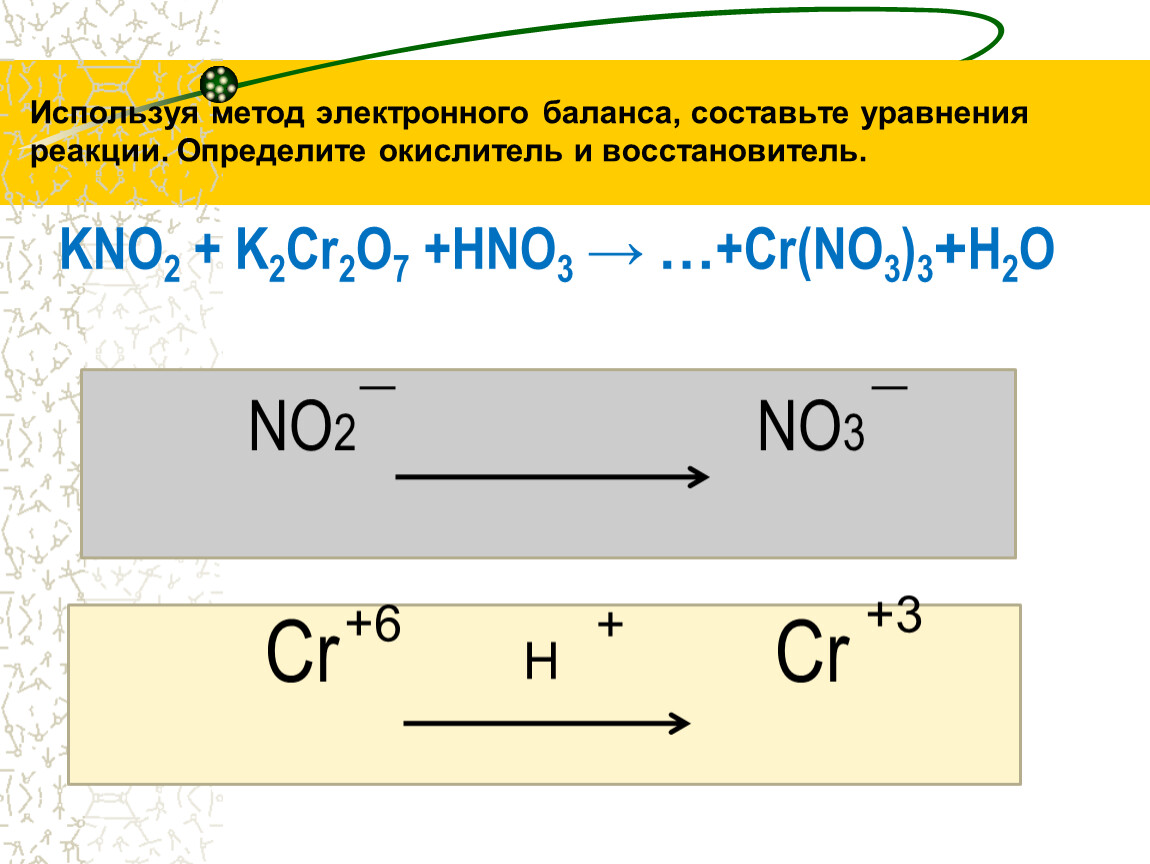
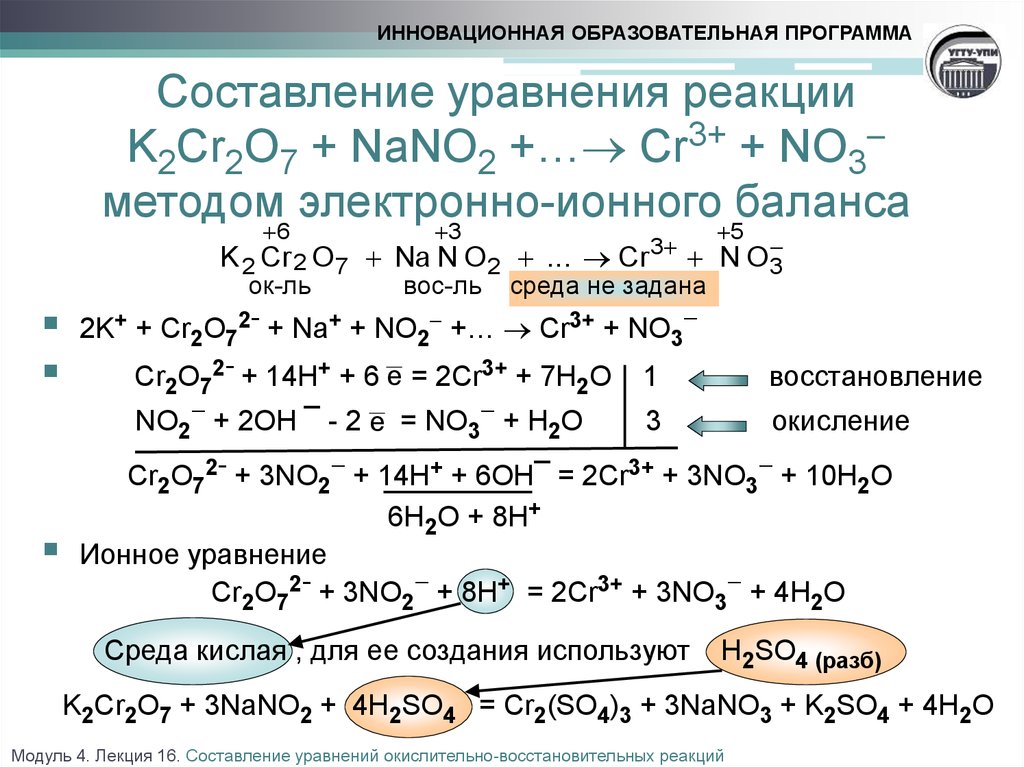
Используя метод электронного баланса, составьте уравнения реакций, соответствующие следующим превращениям: Определите окислители и восстановители. *Цитирирование задания со ссылкой на учебник производится исключительно в учебных целях для …
Используя метод электронного баланса, составьте уравнения реакций, соответствующие следующим превращениям: Определите окислители и восстановители. *Цитирирование задания со ссылкой на учебник производится исключительно в учебных целях для …
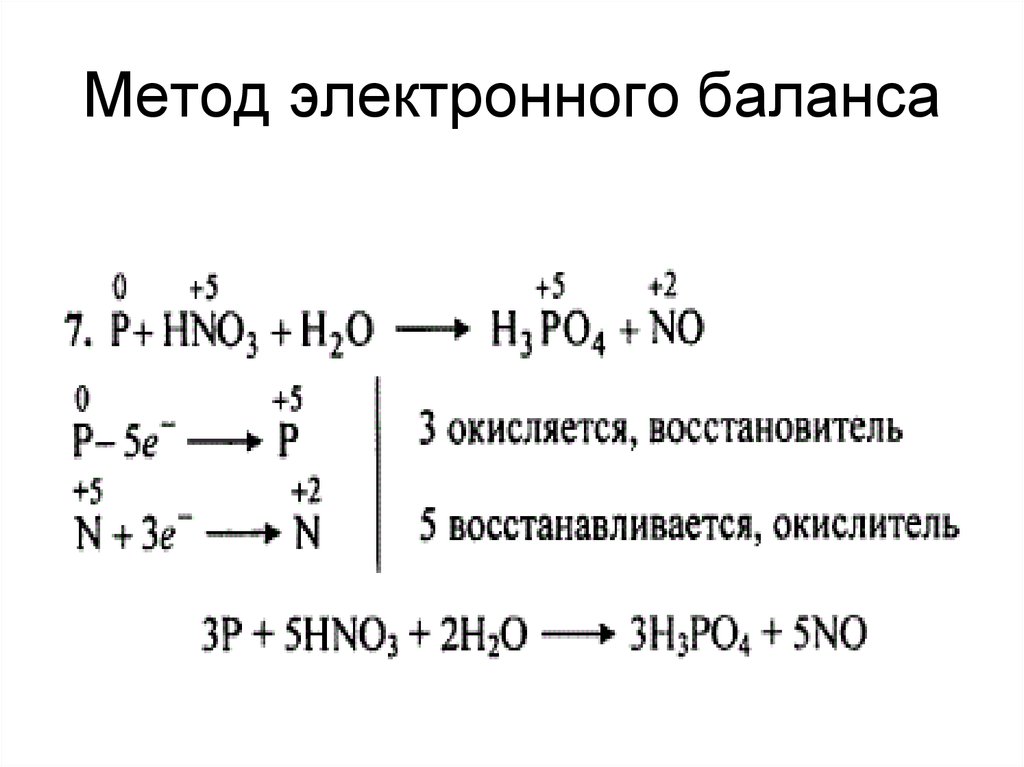
 Используя метод электронного баланса, составьте уравнение реакции, протекающей по схеме: P + HNO3 + H2O > H3PO4 + NO.
Используя метод электронного баланса, составьте уравнение реакции, протекающей по схеме: P + HNO3 + H2O > H3PO4 + NO.
 Используя метод электронного баланса, составьте уравнения реакций, соответствующие следующим превращениям: Укажите окислители и восстановители. *Цитирирование задания со ссылкой на учебник …
Используя метод электронного баланса, составьте уравнения реакций, соответствующие следующим превращениям: Укажите окислители и восстановители. *Цитирирование задания со ссылкой на учебник …
 Используя метод электронного баланса, расставьте коэффициенты в уравнении реакции, схема которой Определите окислитель и восстановитель.
Используя метод электронного баланса, расставьте коэффициенты в уравнении реакции, схема которой Определите окислитель и восстановитель.
 Используя метод электронного баланса, составьте уравнение реакции: feso4 + kclo3 + koh → k2feo4 + kcl + k2so4 + h2o Определите окислитель и восстановитель.
Используя метод электронного баланса, составьте уравнение реакции: feso4 + kclo3 + koh → k2feo4 + kcl + k2so4 + h2o Определите окислитель и восстановитель.
 Для составления уравнений, описывающих такого типа процесс, используют метод электронного баланса. Примеры заданий предполагают, что в любой реакции, которую можно описать способом …
Для составления уравнений, описывающих такого типа процесс, используют метод электронного баланса. Примеры заданий предполагают, что в любой реакции, которую можно описать способом …
 Способ электронного баланса предназначен для облегчения решения заданий по уравниванию двух частей уравнения. В его сути лежит возможность расстановки коэффициентов для окислительно …
Способ электронного баланса предназначен для облегчения решения заданий по уравниванию двух частей уравнения. В его сути лежит возможность расстановки коэффициентов для окислительно …
 Используя метод электронного баланса, составьте уравнения реакций, укажите окислитель и восстановитель: 1.Cr2(SO4)3 +… + NaOH → Na2CrO4 + NaBr + … + H2O
Используя метод электронного баланса, составьте уравнения реакций, укажите окислитель и восстановитель: 1.Cr2(SO4)3 +… + NaOH → Na2CrO4 + NaBr + … + H2O
 Используя метод электронного баланса, составьте уравнение реакции H2SO4 + Zn → ZnSO4 + H2S + H2O Определите окислитель и восстановитель.
Используя метод электронного баланса, составьте уравнение реакции H2SO4 + Zn → ZnSO4 + H2S + H2O Определите окислитель и восстановитель.
 Используя метод электронного баланса, составьте уравнение реакции FeS + HNO 3 конц → … + H 2 SO 4 + NO 2 + …. Определите окислитель и восстановитель.
Используя метод электронного баланса, составьте уравнение реакции FeS + HNO 3 конц → … + H 2 SO 4 + NO 2 + …. Определите окислитель и восстановитель.
 Для реакции, схема которой MnO2 + KClO3 + KOH ( K2MnO4 + KCl + H2O. методом ионно-электронного баланса расставить коэффициенты. Решение. 1-я полуреакция: MnO2 – …
Для реакции, схема которой MnO2 + KClO3 + KOH ( K2MnO4 + KCl + H2O. методом ионно-электронного баланса расставить коэффициенты. Решение. 1-я полуреакция: MnO2 – …
 Используя метод электронного баланса, составьте уравнения реакций, соответствующие следующим схемам: а) Ва + N2 -> Ba3N2. б) Са + Н2O -> Са (ОН)2 + Н2. в) А1 + HCl -> …
Используя метод электронного баланса, составьте уравнения реакций, соответствующие следующим схемам: а) Ва + N2 -> Ba3N2. б) Са + Н2O -> Са (ОН)2 + Н2. в) А1 + HCl -> …
 Используя метод электронного баланса, составьте уравнение реакции: Определите окислитель и восстановитель. Показать разбор
Используя метод электронного баланса, составьте уравнение реакции: Определите окислитель и восстановитель. Показать разбор
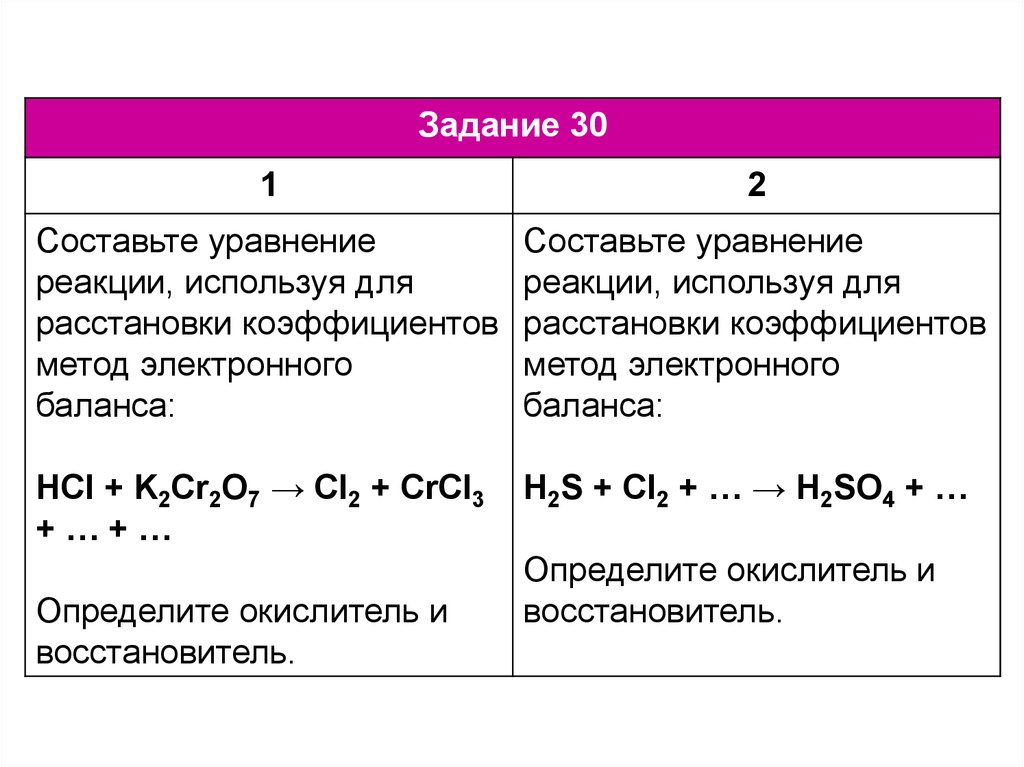
 Расставлены коэффициенты в уравнении реакции: 3. Указано, что сера в степени окисления (или сероводород за счет серы в степени окисления ) является …
Расставлены коэффициенты в уравнении реакции: 3. Указано, что сера в степени окисления (или сероводород за счет серы в степени окисления ) является …
 Просуммируем порознь левые и правые части полу реакций: -2 +5 0 +4 2o + 4n = o2 + 4n. Теперь расставим коэффициенты в уравнение: 4HNO3 = 2H2O + 4NO2 + O2.
Просуммируем порознь левые и правые части полу реакций: -2 +5 0 +4 2o + 4n = o2 + 4n. Теперь расставим коэффициенты в уравнение: 4HNO3 = 2H2O + 4NO2 + O2.
 Используя метод электронного баланса, составьте уравнение реакции, соответствующее следующей схеме: Al + HNO3 -> Al(NO3)3 + N2O + Н2O
Используя метод электронного баланса, составьте уравнение реакции, соответствующее следующей схеме: Al + HNO3 -> Al(NO3)3 + N2O + Н2O
Еще по теме:

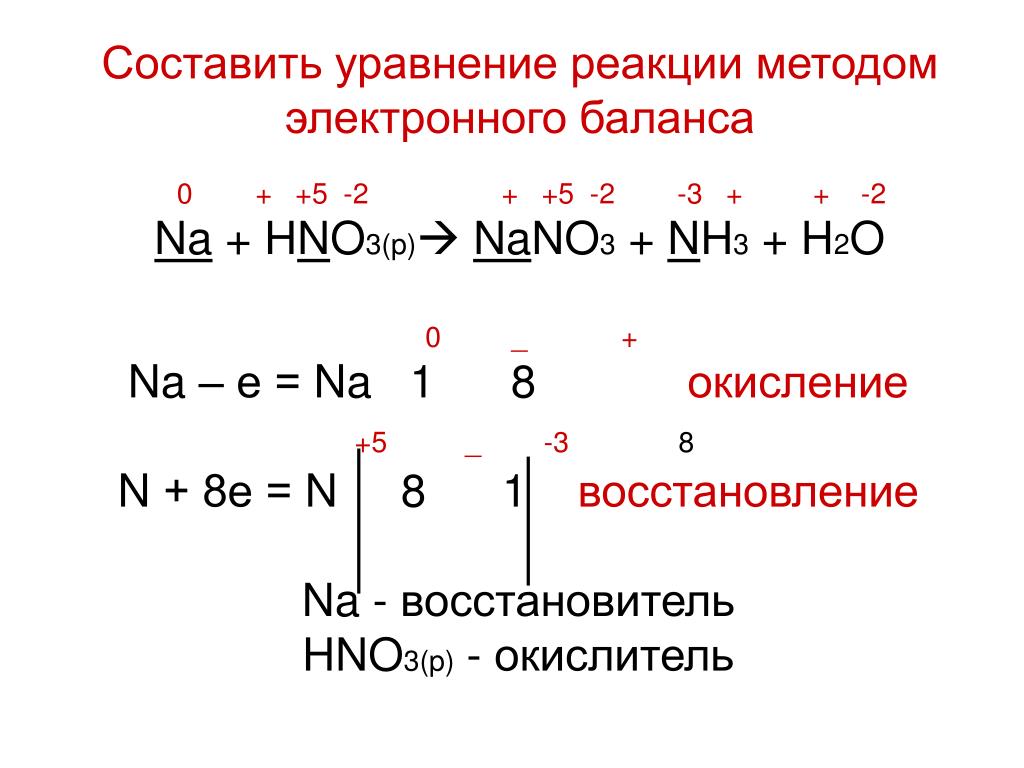











Еще по теме: