2 Cr (O H)3 + 3 Cl 2 + 10 K O H → 8 H 2 O + 2 K 2 Cr O 4 + 6 K Cl. Это кислотно-щелочная реакция (нейтрализа́ция): Cr(OH)3 представляет собой кислоту, KOH является …
2 Cr (O H)3 + 3 Cl 2 + 10 K O H → 8 H 2 O + 2 K 2 Cr O 4 + 6 K Cl. Это кислотно-щелочная реакция (нейтрализа́ция): Cr(OH)3 представляет собой кислоту, KOH является …
 Решенное и коэффициентами уравнение реакции 2 Cr (OH)3 + 10 KOH + 3 Cl2 → 6 KCl + 2 K2CrO4 + 8 H2O с дополненными продуктами.
Решенное и коэффициентами уравнение реакции 2 Cr (OH)3 + 10 KOH + 3 Cl2 → 6 KCl + 2 K2CrO4 + 8 H2O с дополненными продуктами.
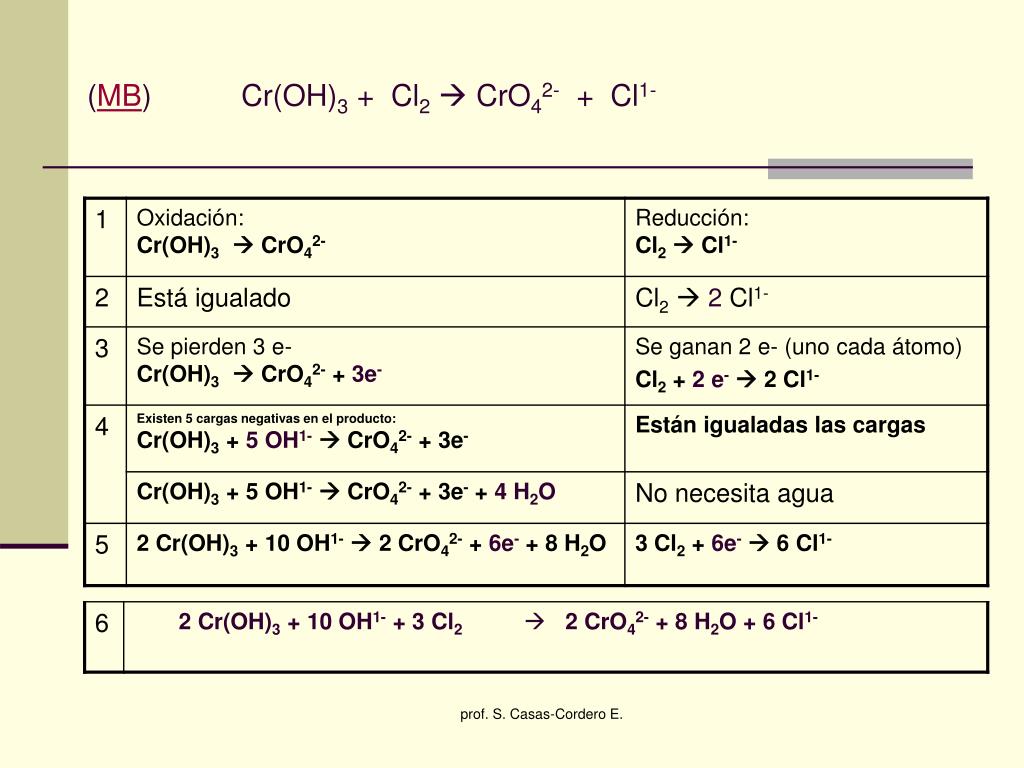
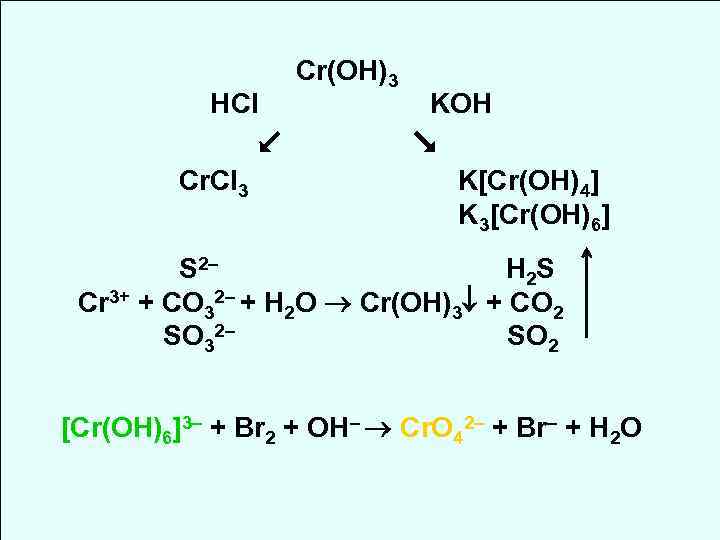 Cr(OH)3 + Cl2 + KOH = … + … + … Укажите окислитель и восстановитель.
Cr(OH)3 + Cl2 + KOH = … + … + … Укажите окислитель и восстановитель.
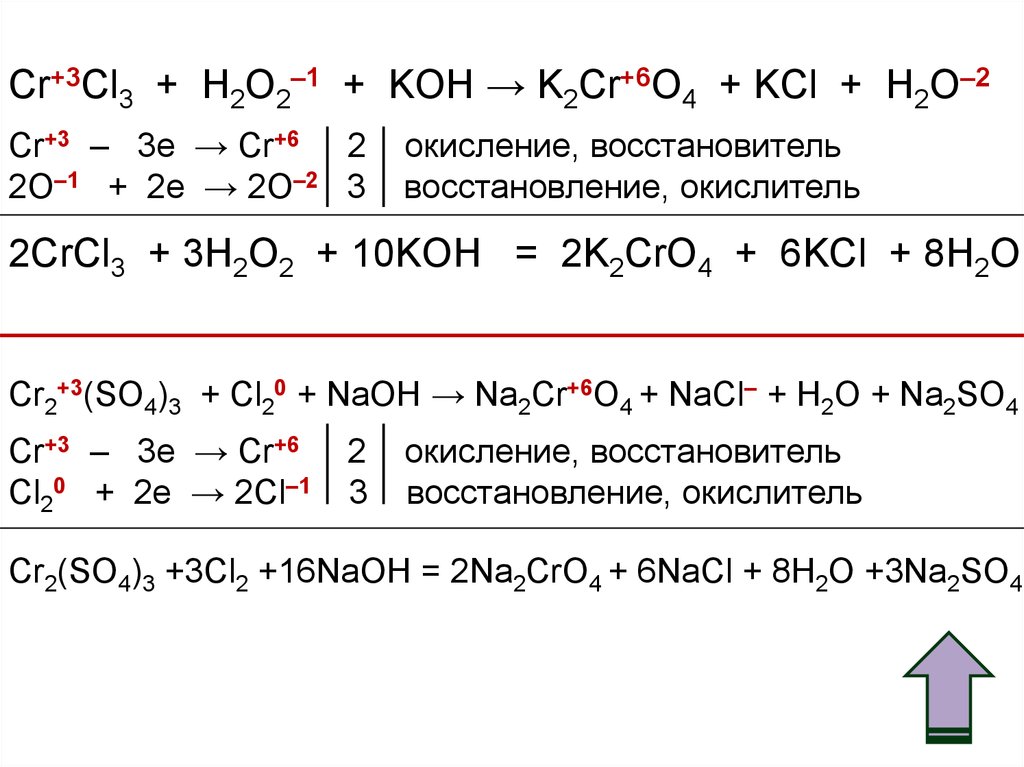 Balance the reaction of Cr(OH)3 + Cl2 + KOH = KCl + K2CrO4 + H2O using this chemical equation balancer!
Balance the reaction of Cr(OH)3 + Cl2 + KOH = KCl + K2CrO4 + H2O using this chemical equation balancer!
 Расширенный поиск. Или Попробуйте случайную реакцию. Приложение для вычисления и дополнения продуктов реакции. Ионные и окислительно-восстановительные реакции!
Расширенный поиск. Или Попробуйте случайную реакцию. Приложение для вычисления и дополнения продуктов реакции. Ионные и окислительно-восстановительные реакции!
 Чему равна степень окисления азота в азотистой кислоте HNO2? +3 +2 +1 +5 2. Какая реакция является окислительно-восстановительной? HCl + NaOH = NaCl+H2O 2H2.
Чему равна степень окисления азота в азотистой кислоте HNO2? +3 +2 +1 +5 2. Какая реакция является окислительно-восстановительной? HCl + NaOH = NaCl+H2O 2H2.
 A. Cho dung dịch NaOH đến dư vào dung dịch Cr(NO 3) 3. B. Cho dung dịch HCl đến dư vào dung dịch NaAlO 2 (hoặc Na[Al(OH) 4 ]) C. Thổi CO 2 đến dư vào dung dịch Ca(OH) 2 .
A. Cho dung dịch NaOH đến dư vào dung dịch Cr(NO 3) 3. B. Cho dung dịch HCl đến dư vào dung dịch NaAlO 2 (hoặc Na[Al(OH) 4 ]) C. Thổi CO 2 đến dư vào dung dịch Ca(OH) 2 .
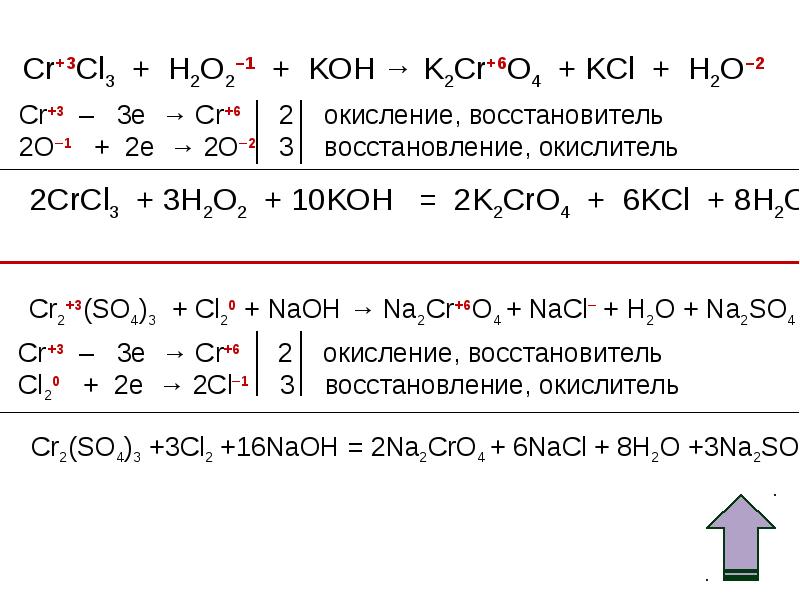 Balance the reaction of CrCl3 + KOH = Cr(OH)3 + KCl using this chemical equation balancer!
Balance the reaction of CrCl3 + KOH = Cr(OH)3 + KCl using this chemical equation balancer!
 Для решения овр такого типа нужно просто натренироваться, для этого предлагаю вам решить следующие овр методом полуреакций: MnO 2 + O 2 + KOH → …. …
Для решения овр такого типа нужно просто натренироваться, для этого предлагаю вам решить следующие овр методом полуреакций: MnO 2 + O 2 + KOH → …. …
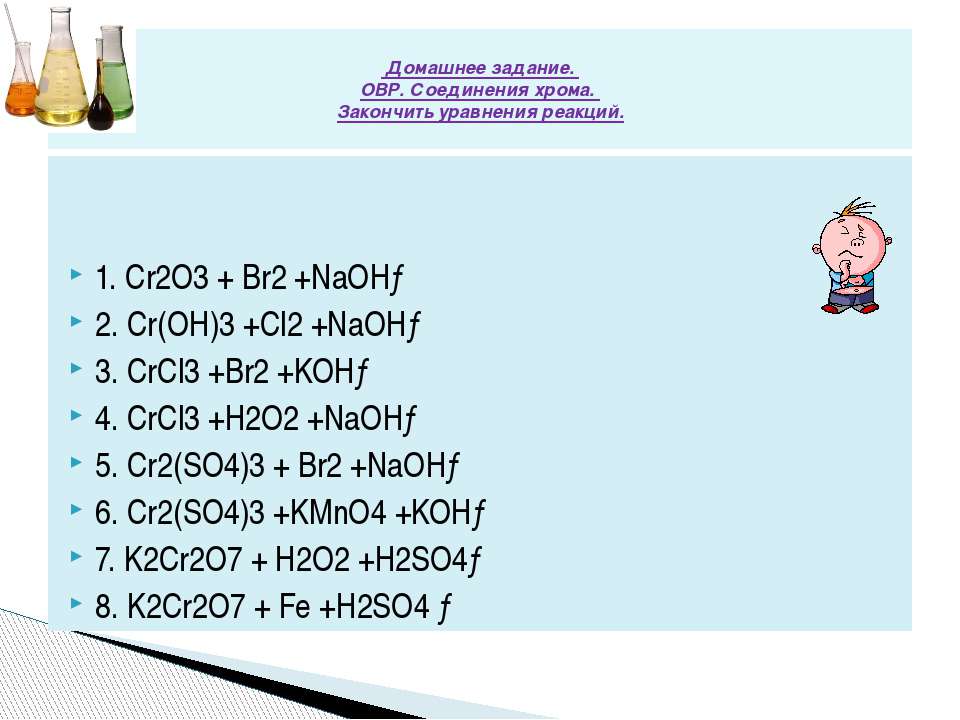 Решенное и коэффициентами уравнение реакции 2 CrCl3 + 16 KOH + 3 Cl2 → 12 KCl + 2 K2CrO4 + 8 H2O с дополненными продуктами. Приложение для вычисления и …
Решенное и коэффициентами уравнение реакции 2 CrCl3 + 16 KOH + 3 Cl2 → 12 KCl + 2 K2CrO4 + 8 H2O с дополненными продуктами. Приложение для вычисления и …
 Хромит калия — соль калия и слабой несуществующей хромистой кислоты с формулой KCrO2. Также может рассматриваться как смешанный окисел K2O•Cr2O3. Твёрдое …
Хромит калия — соль калия и слабой несуществующей хромистой кислоты с формулой KCrO2. Также может рассматриваться как смешанный окисел K2O•Cr2O3. Твёрдое …
 To enter an ion, specify charge after the compound in curly brackets: {+3} or {3+} or {3}. Example: Fe{3+} + I{-} = Fe{2+} + I2; Substitute immutable groups in chemical compounds to avoid …
To enter an ion, specify charge after the compound in curly brackets: {+3} or {3+} or {3}. Example: Fe{3+} + I{-} = Fe{2+} + I2; Substitute immutable groups in chemical compounds to avoid …
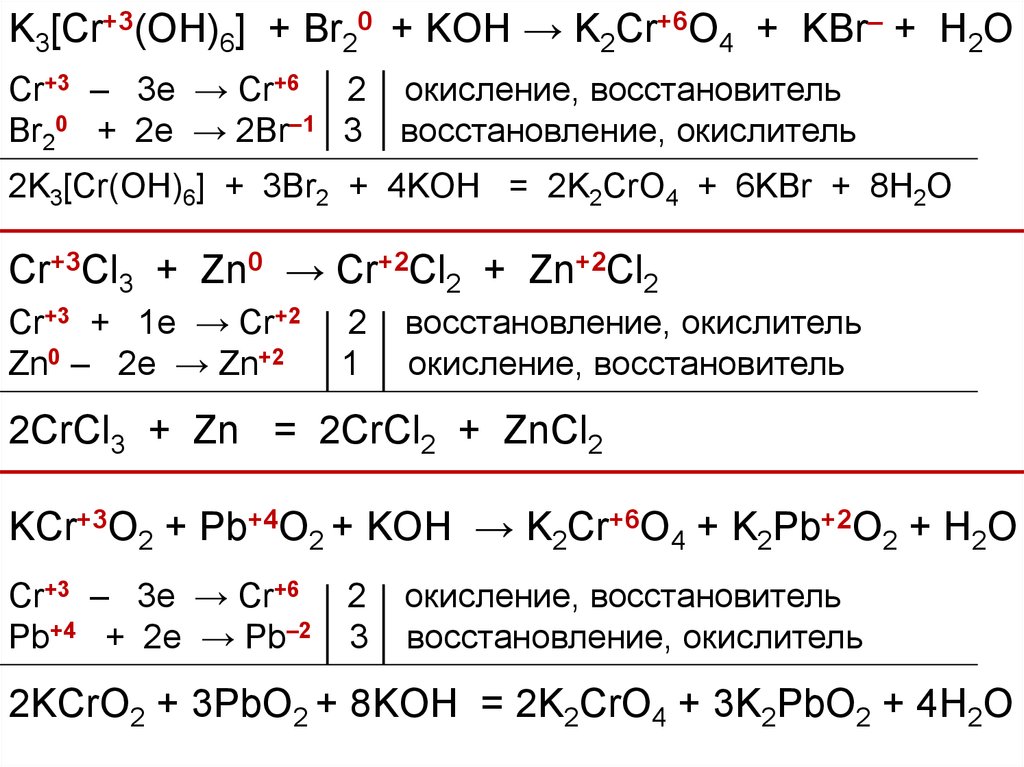 CrCl 3 + 3KOH (недост) → Cr(OH) 3 ↓ + 3KCl 4. Также гидроксид хрома (III) образуется при взаимодействии растворимых солей хрома (III) с растворимыми …
CrCl 3 + 3KOH (недост) → Cr(OH) 3 ↓ + 3KCl 4. Также гидроксид хрома (III) образуется при взаимодействии растворимых солей хрома (III) с растворимыми …
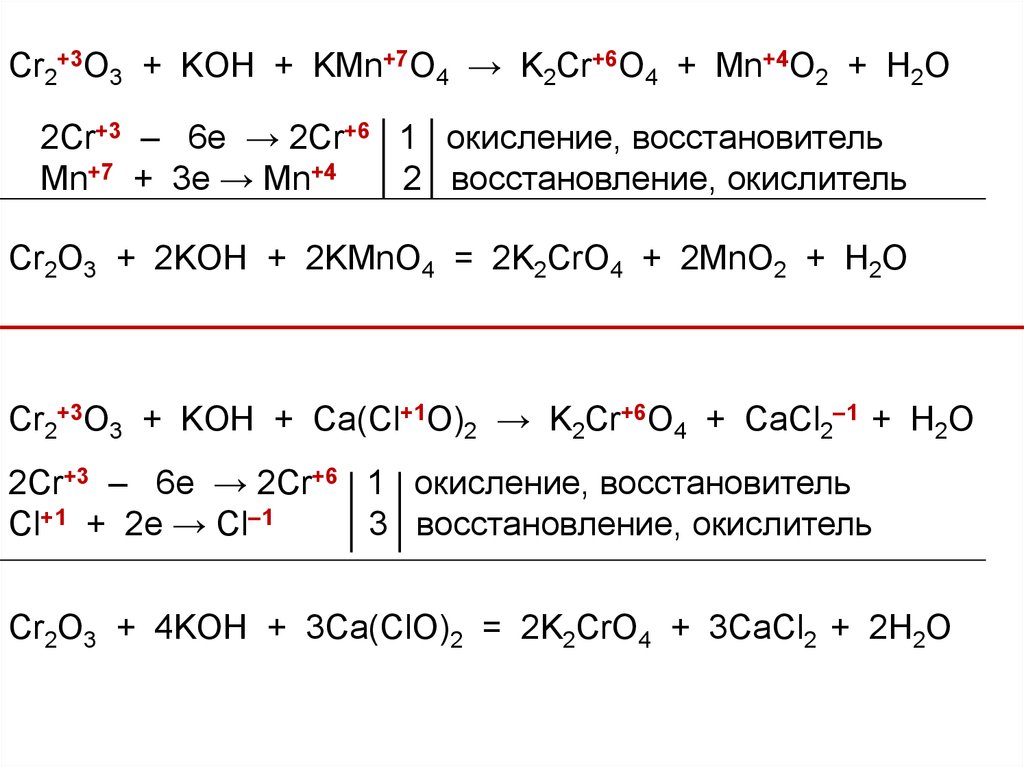 A chemical equation represents a chemical reaction. It shows the reactants (substances that start a reaction) and products (substances formed by the reaction). For example, in the reaction of …
A chemical equation represents a chemical reaction. It shows the reactants (substances that start a reaction) and products (substances formed by the reaction). For example, in the reaction of …
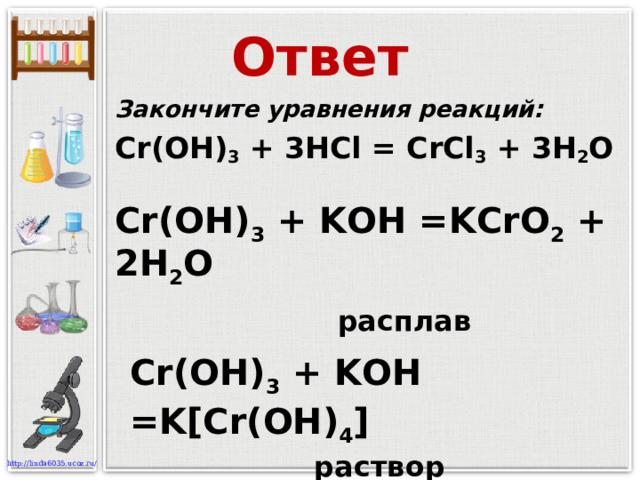 Phosphorus goes from 0 to -3, gaining 3 electrons (reduction). Balance the changes using electrons: Multiply the number of calcium atoms by 3 and the number of phosphorus atoms by …
Phosphorus goes from 0 to -3, gaining 3 electrons (reduction). Balance the changes using electrons: Multiply the number of calcium atoms by 3 and the number of phosphorus atoms by …
Еще по теме:


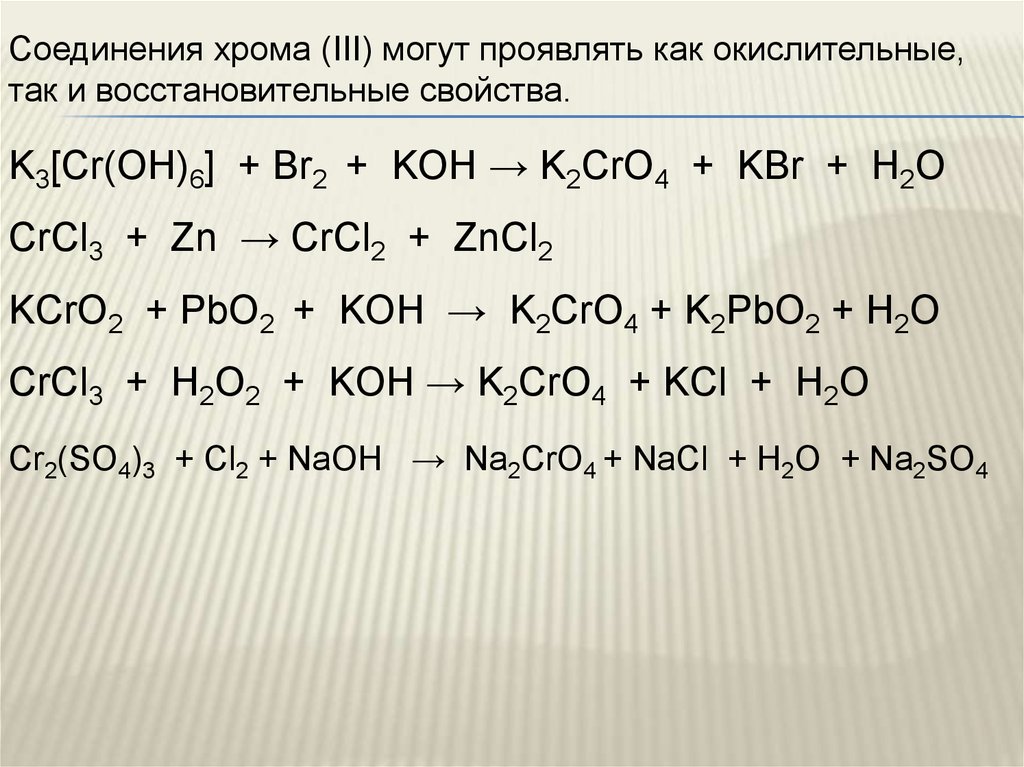
![Cr2 (SO4)3 + 12 KOH → 2 K3 [Cr (OH)6] + 3 K2SO4 Foto 19](https://i.sstatic.net/KTuH2.png)



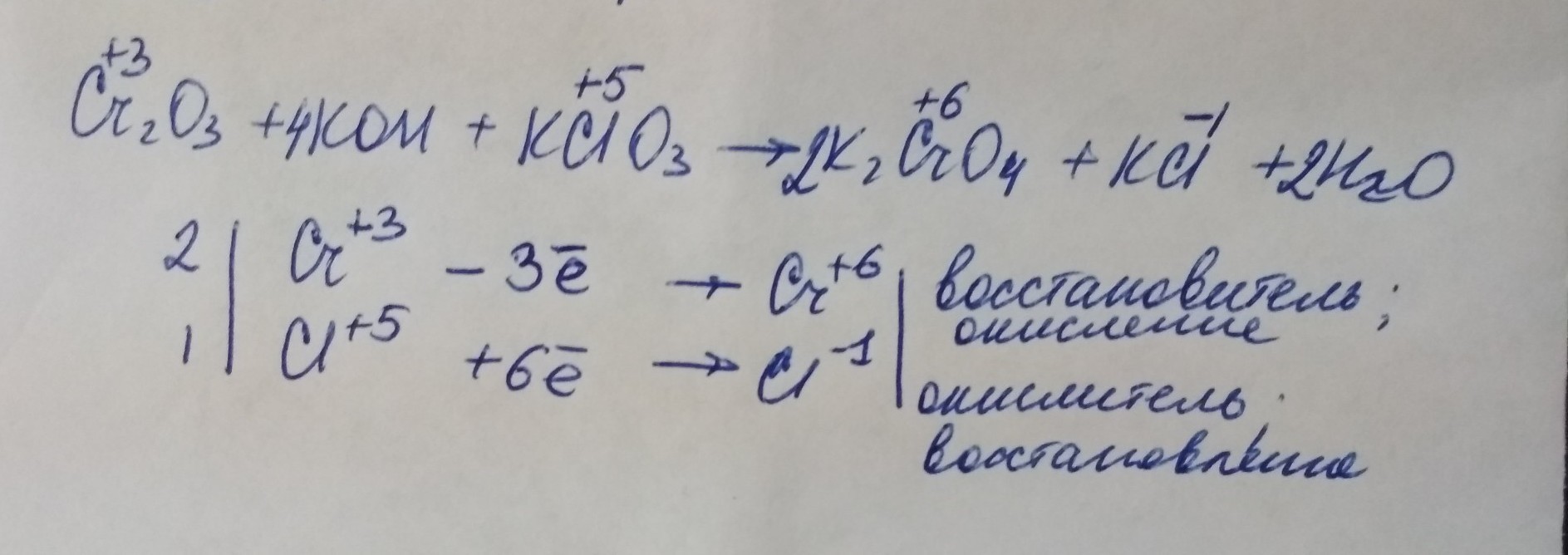


Еще по теме: