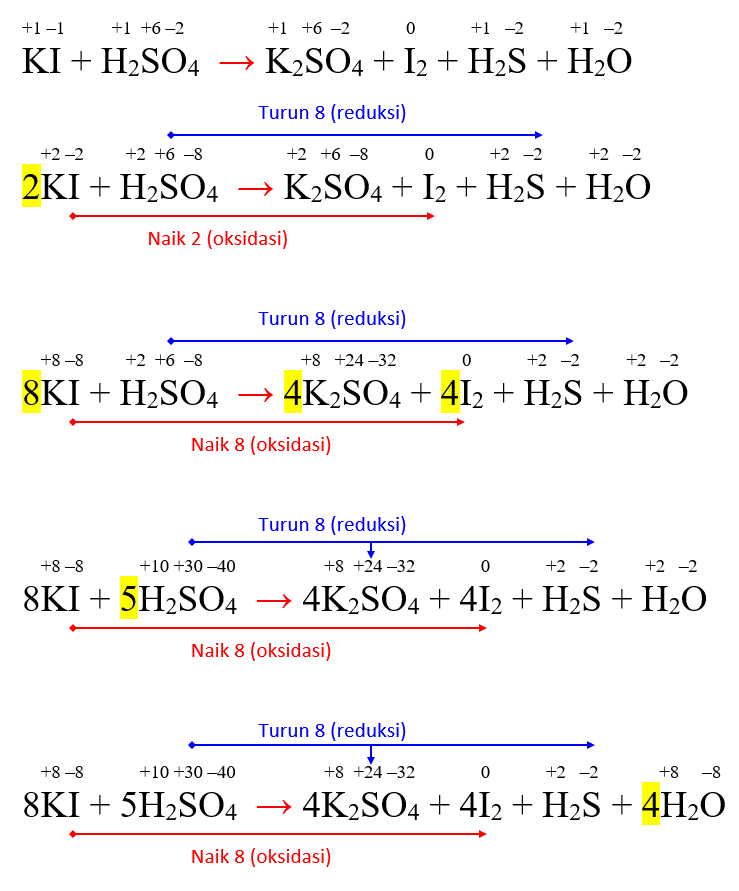
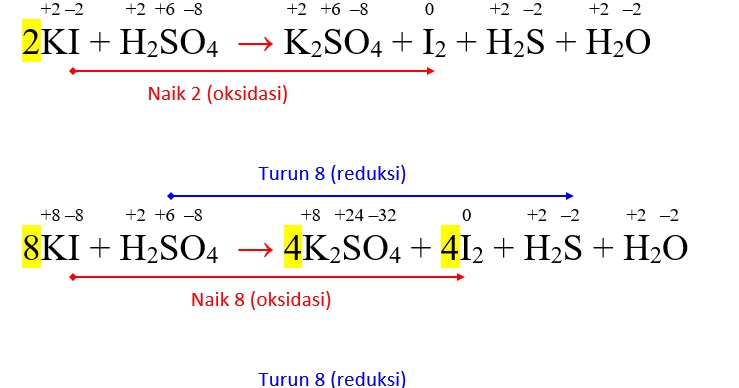
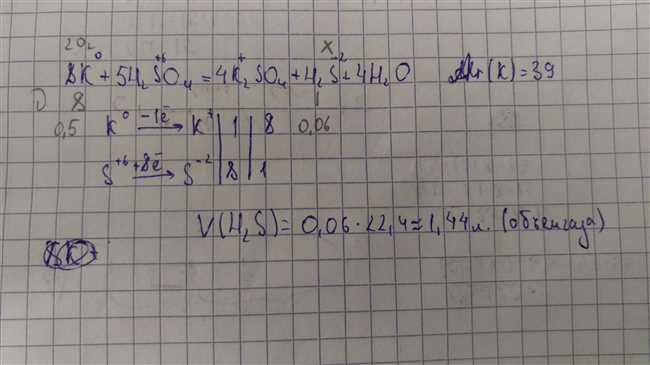 Решенное и коэффициентами уравнение реакции 8 KI + 5 H2SO4 → 4 I2 + 4 K2SO4 + H2S + 4 H2O с дополненными продуктами. Приложение для вычисления и дополнения …
Решенное и коэффициентами уравнение реакции 8 KI + 5 H2SO4 → 4 I2 + 4 K2SO4 + H2S + 4 H2O с дополненными продуктами. Приложение для вычисления и дополнения …
 Решенное и коэффициентами уравнение реакции H2SO4 + KI + KIO → H2O + K2SO4 + I2 с дополненными продуктами. Приложение для вычисления и дополнения продуктов реакции.
Решенное и коэффициентами уравнение реакции H2SO4 + KI + KIO → H2O + K2SO4 + I2 с дополненными продуктами. Приложение для вычисления и дополнения продуктов реакции.
 KI + H2SO4 (конц) = I2 + S + K2SO4 +.. Закончите уравнение реакции, расставьте коэффициенты методом электронного баланса. KI + H2SO4 (конц) = I2 + S + …
KI + H2SO4 (конц) = I2 + S + K2SO4 +.. Закончите уравнение реакции, расставьте коэффициенты методом электронного баланса. KI + H2SO4 (конц) = I2 + S + …
 Химические Уравнения oнлайн! Приложение для вычисления и дополнения продуктов реакции. Ионные и окислительно-восстановительные реакции!
Химические Уравнения oнлайн! Приложение для вычисления и дополнения продуктов реакции. Ионные и окислительно-восстановительные реакции!
 Balance the reaction of KI + H2SO4 = K2SO4 + I2 + H2S + H2O using this chemical equation balancer!
Balance the reaction of KI + H2SO4 = K2SO4 + I2 + H2S + H2O using this chemical equation balancer!
 Йодид калия является более сильным окислителем и восстановит серную кислоту до сероводорода (h2s): 8kj + 5h2so4(конц.
Йодид калия является более сильным окислителем и восстановит серную кислоту до сероводорода (h2s): 8kj + 5h2so4(конц.
 8ki(т) + 9h2so4 (конц. ) = 4i2↓+ h2s↑ + 4h2o + 8khso4 или так: 5h2so4(конц. ) + 8ki(т) = h2s↑ + 4i2↓ + 4h2o + 4k2so4
8ki(т) + 9h2so4 (конц. ) = 4i2↓+ h2s↑ + 4h2o + 8khso4 или так: 5h2so4(конц. ) + 8ki(т) = h2s↑ + 4i2↓ + 4h2o + 4k2so4
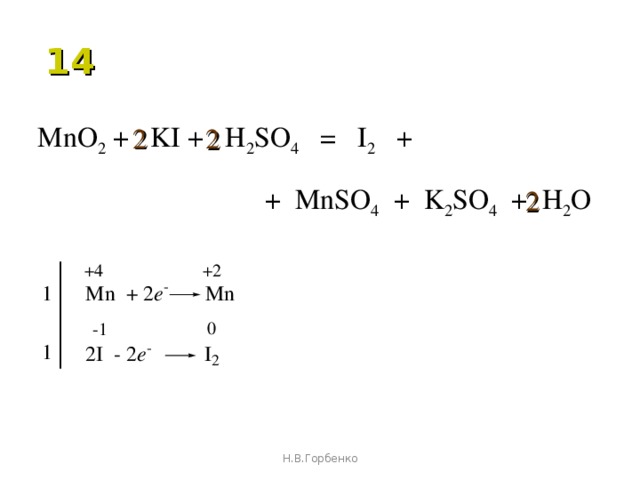 напишите продукты реакции (протекает при нагревании): KI + H2SO4 (конц) - ответ на этот и другие вопросы получите онлайн на сайте Uchi.ru
напишите продукты реакции (протекает при нагревании): KI + H2SO4 (конц) - ответ на этот и другие вопросы получите онлайн на сайте Uchi.ru
 Методом ионно-электронных уравнений подберите коэффициенты в следующих окислительно-восстановительных реакциях. 1)Al + K2Cr2O7 + H2SO4→ Al2 (SO4)3 + Cr2 …
Методом ионно-электронных уравнений подберите коэффициенты в следующих окислительно-восстановительных реакциях. 1)Al + K2Cr2O7 + H2SO4→ Al2 (SO4)3 + Cr2 …
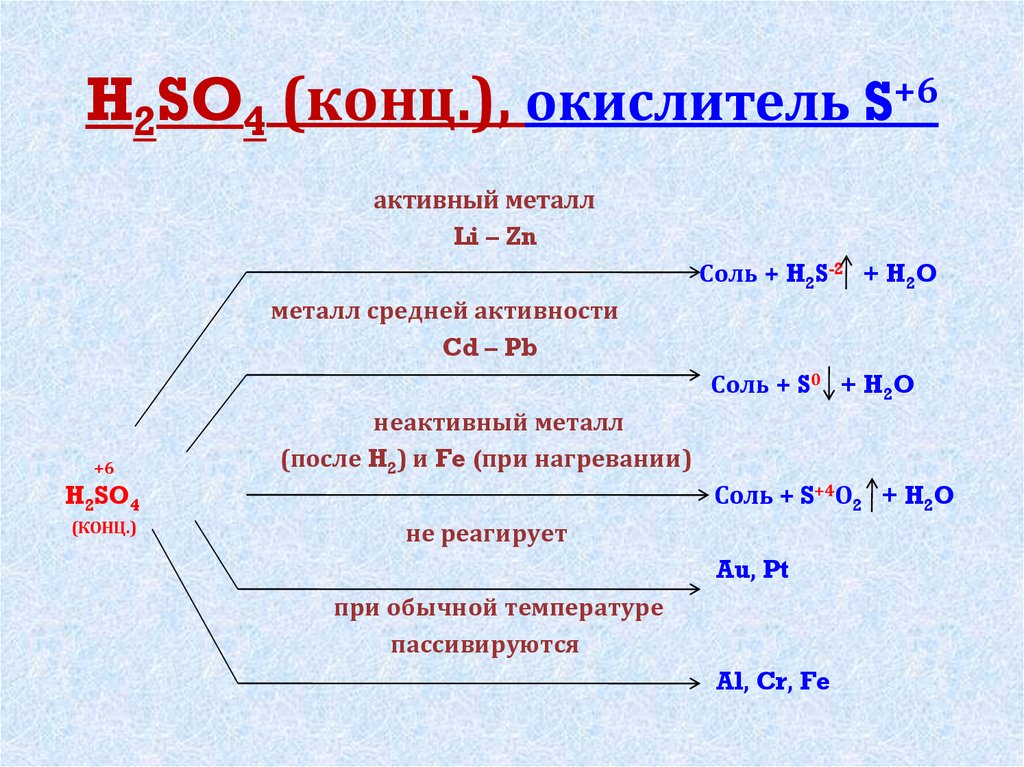
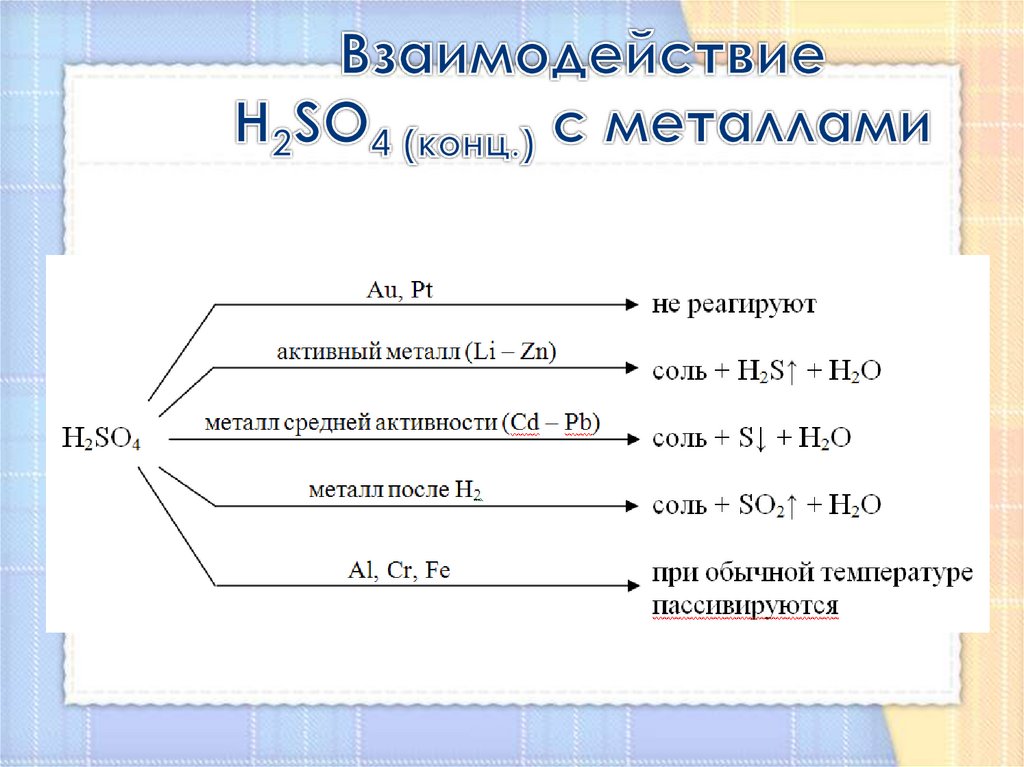
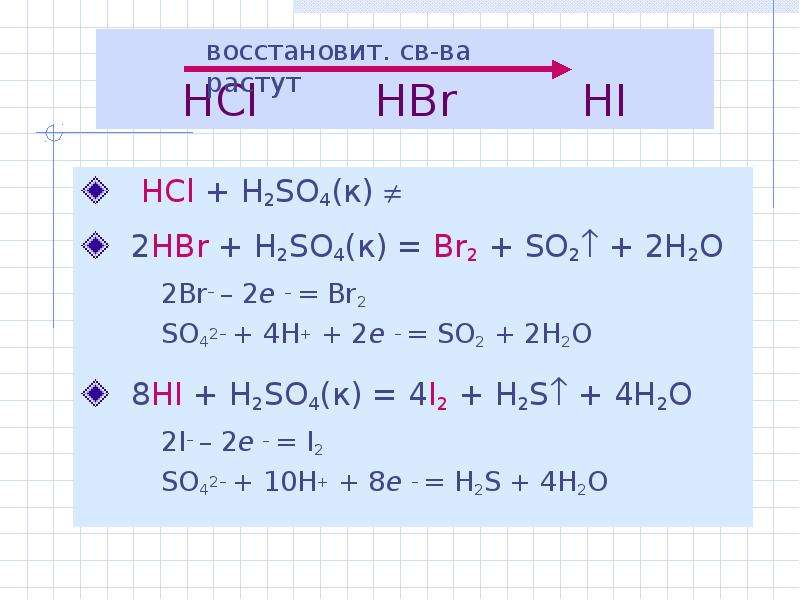
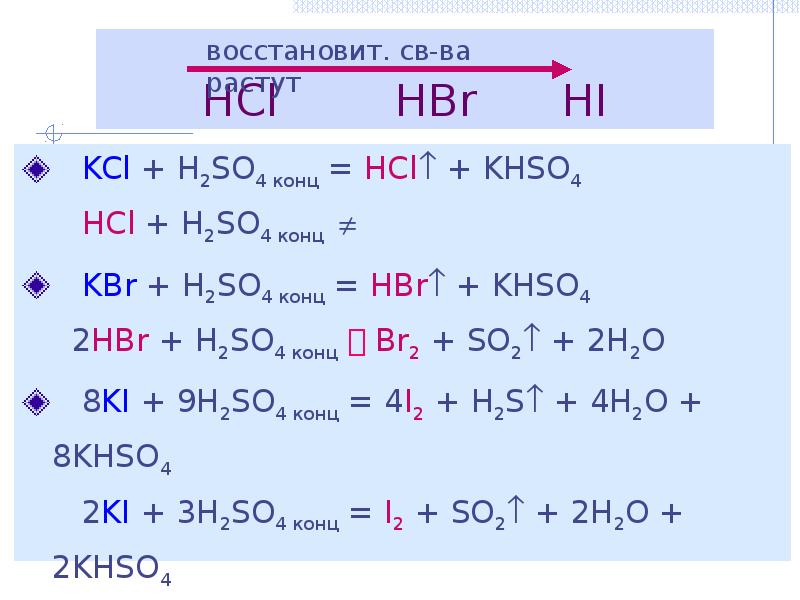 При взаимодействии h2so4(конц.) с сильными восстановителями (активными металлами: li-zn, некоторыми сложными веществами: hi, ki) образуются h2s или s.
При взаимодействии h2so4(конц.) с сильными восстановителями (активными металлами: li-zn, некоторыми сложными веществами: hi, ki) образуются h2s или s.
 Решенное и коэффициентами уравнение реакции K2Cr2O7 + 6 KI + 7 H2SO4 → 4 K2SO4 + Cr2 (SO4)3 + 3 I2 + 7 H2O с дополненными продуктами. Приложение для вычисления и …
Решенное и коэффициентами уравнение реакции K2Cr2O7 + 6 KI + 7 H2SO4 → 4 K2SO4 + Cr2 (SO4)3 + 3 I2 + 7 H2O с дополненными продуктами. Приложение для вычисления и …
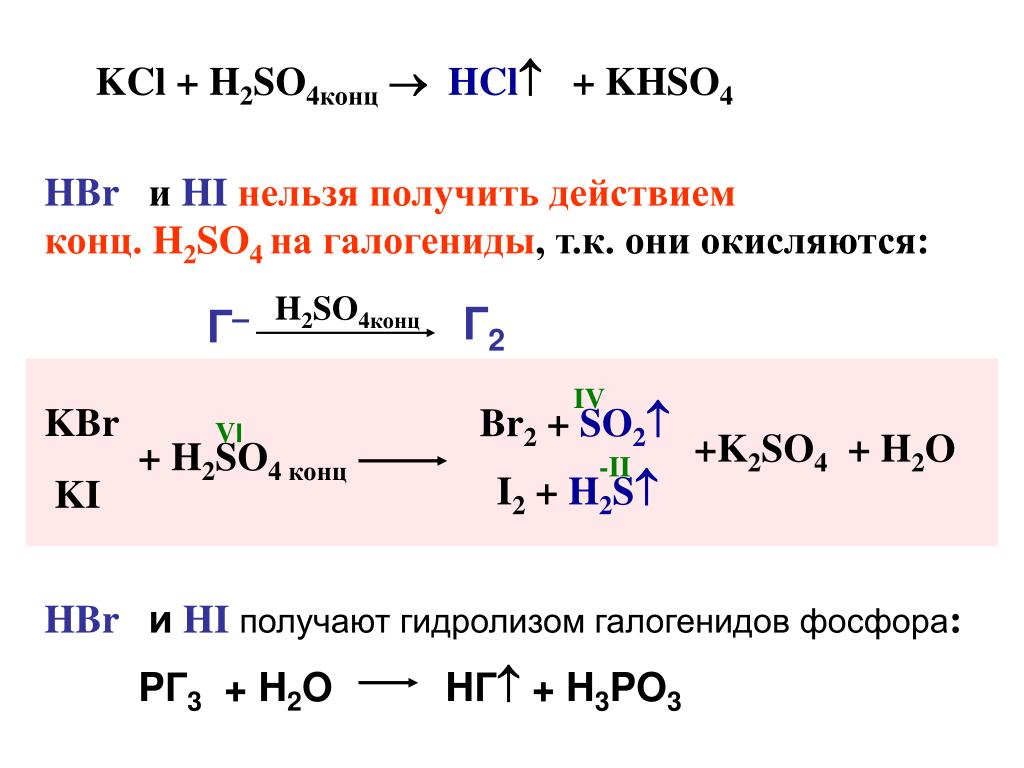 Сокращаем одинаковые молекулы слева и справа: Метод полуреакций удобен тем, что можно легко предсказать продукты реакции и сочетания ионов. Да и уравнивать …
Сокращаем одинаковые молекулы слева и справа: Метод полуреакций удобен тем, что можно легко предсказать продукты реакции и сочетания ионов. Да и уравнивать …
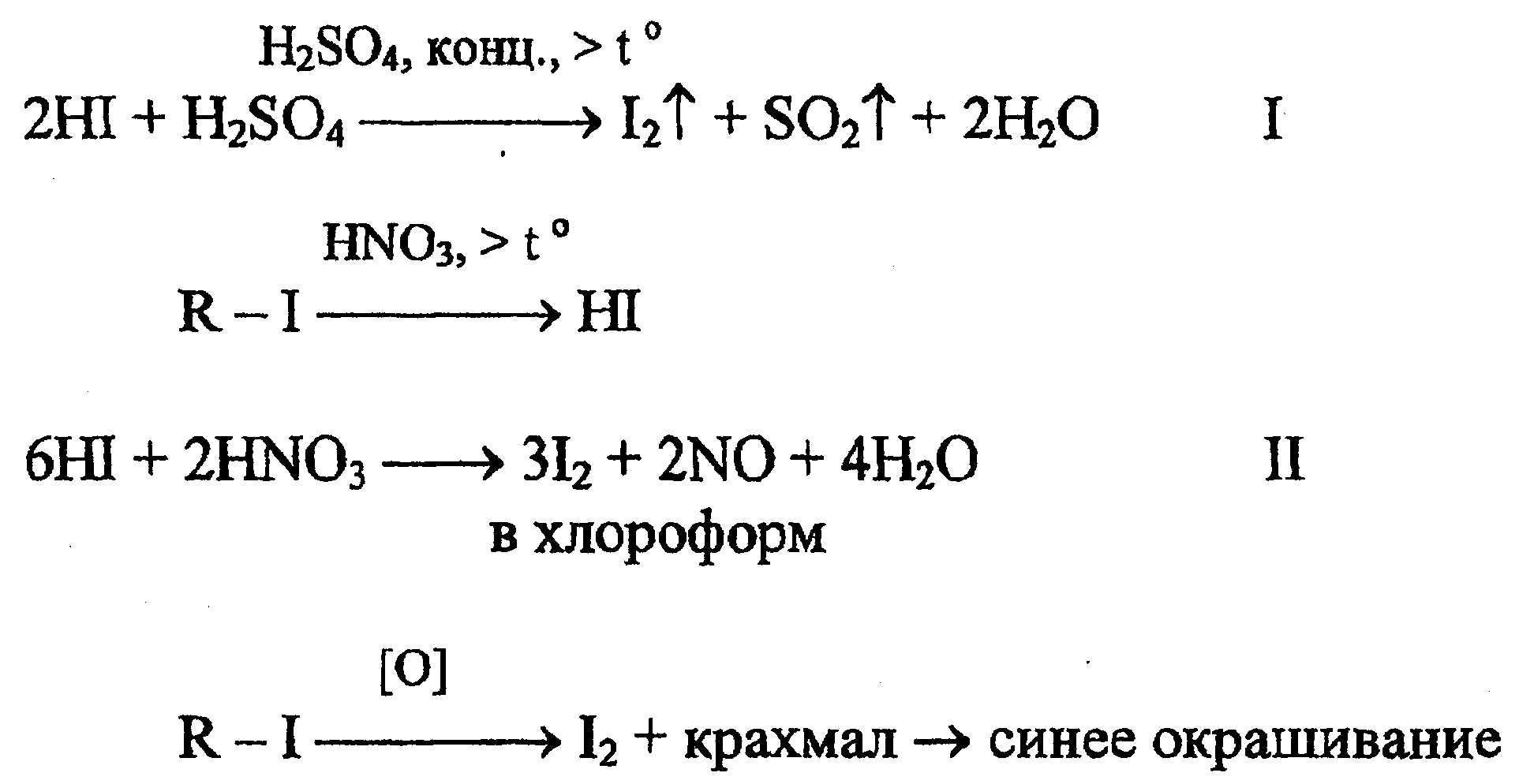
 Окисление соединений S–2 до S+6 происходит под действием следующих окислителей: H2O2, Cl2(водн.), HNO3(конц.): H 2 S + 8HNO 3 (конц.) → H2SO4 + 8NO 2 + 4H 2 O …
Окисление соединений S–2 до S+6 происходит под действием следующих окислителей: H2O2, Cl2(водн.), HNO3(конц.): H 2 S + 8HNO 3 (конц.) → H2SO4 + 8NO 2 + 4H 2 O …
 В реакциях с H 2 SO 4 (конц.) помимо соли и воды выделяется SO 2. В реакциях с HNO 3 (разб.) помимо соли и воды выделяется NO, тогда как в сдучае HNO 3 (конц.) …
В реакциях с H 2 SO 4 (конц.) помимо соли и воды выделяется SO 2. В реакциях с HNO 3 (разб.) помимо соли и воды выделяется NO, тогда как в сдучае HNO 3 (конц.) …
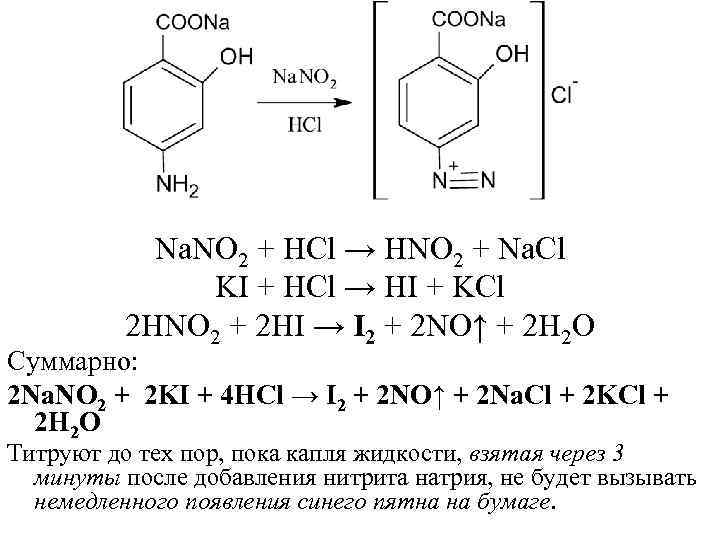
 Решенное и коэффициентами уравнение реакции 2 KNO2 + 2 KI + 2 H2SO4 → 2 NO + I2 + 2 K2SO4 + 2 H2O с дополненными продуктами. Приложение для вычисления и …
Решенное и коэффициентами уравнение реакции 2 KNO2 + 2 KI + 2 H2SO4 → 2 NO + I2 + 2 K2SO4 + 2 H2O с дополненными продуктами. Приложение для вычисления и …
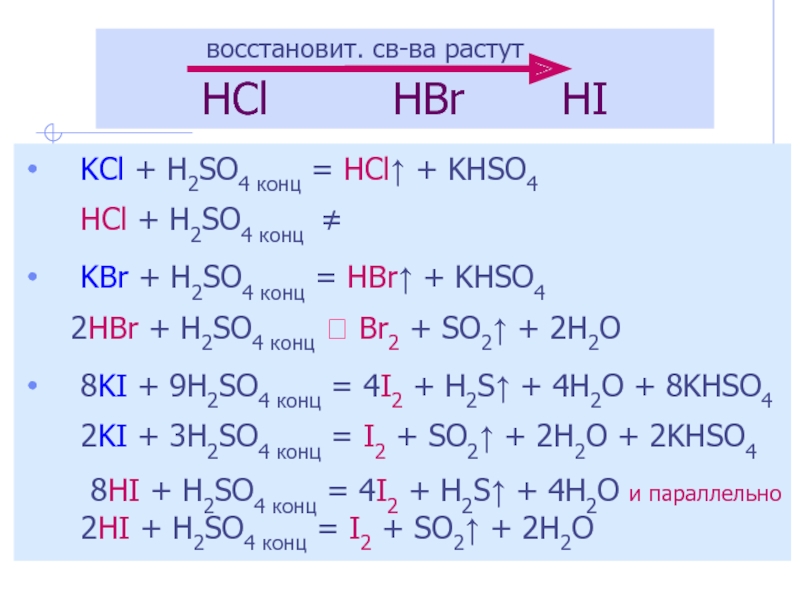 На экзамене по химии написал в С2 : KI+H2SO4 (конц.) = K2SO4+HI. Это неправильно? Котенька. Высший разум (603793) 11 лет назад.
На экзамене по химии написал в С2 : KI+H2SO4 (конц.) = K2SO4+HI. Это неправильно? Котенька. Высший разум (603793) 11 лет назад.
Еще по теме:

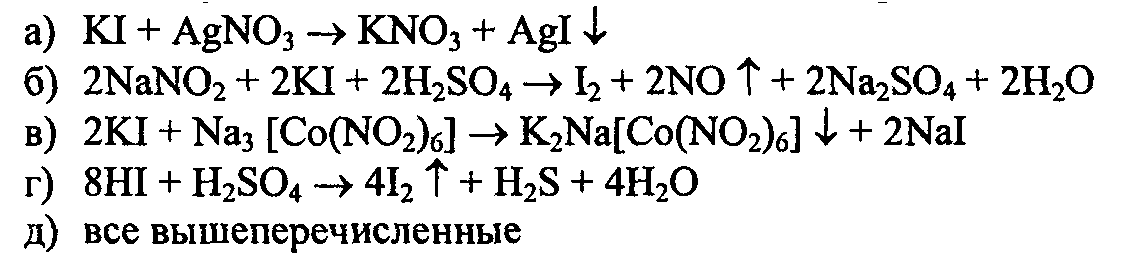
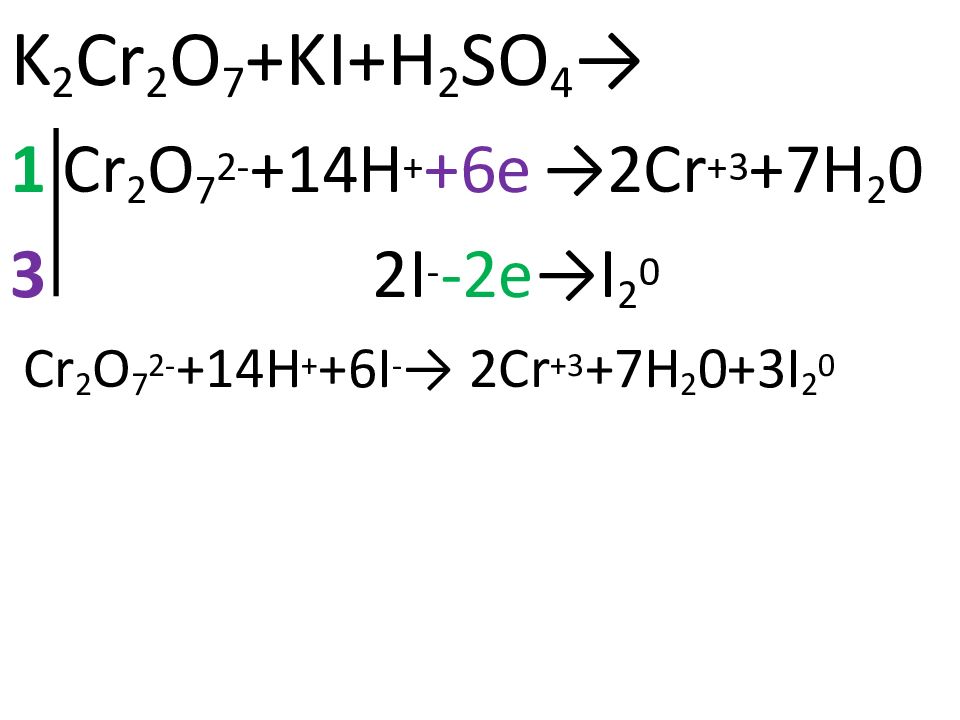
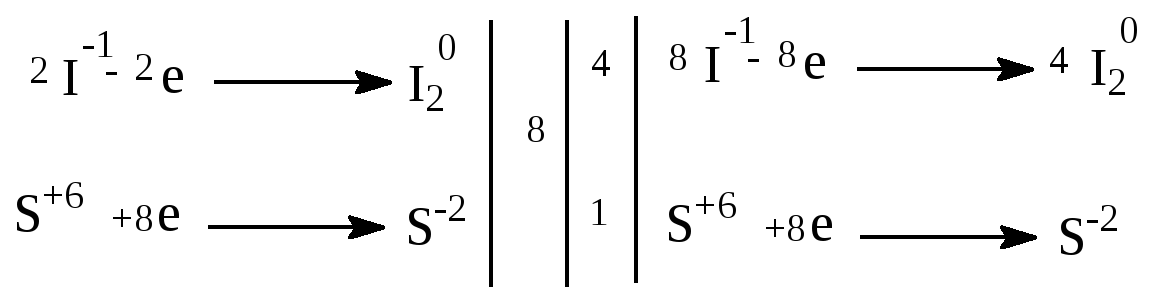









Еще по теме: